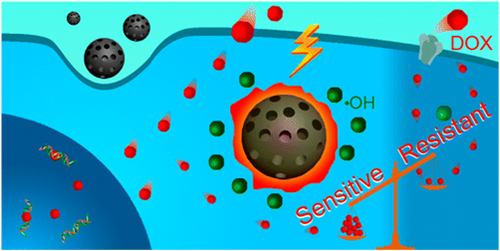
肿瘤耐药是导致化疗失败的主要原因。在长期化疗中,未被药物杀死的肿瘤细胞发生结构和功能变异,对药物不敏感,产生耐药。由于化疗药物的强毒副作用,并不能通过提高药物剂量来抑制耐药,最终导致无药可用。目前,临床仍缺乏治疗耐药的有效途径。据美国癌症协会估计,90%以上肿瘤患者死于不同程度的耐药。肿瘤细胞对阿霉素等药物产生耐药的原因很多,主要包括抑癌基因突变、细胞膜转运蛋白大量表达等,这些原因与耐药细胞的抗氧化系统并呈低氧化还原水平密切相关。
如何设计一种功能性的药物载体,既能实现药物载带和可控释放,又能改变耐药本质,是纳米医学面临的重大挑战。最近,国家纳米科学中心陈春英课题组提出全新策略:用一种新型、球形、空心碳纳米载体,基于光催化性质产生自由基来解决耐药这一科学难题。该纳米载体兼有良好的光催化能力、高效药物载带能力,经短暂激光刺激就能克服肿瘤耐药。研究发现,碳纳米载体表面及介孔通道富含sp2和sp3碳结构,具有电子传递的潜力。激光刺激后,纳米载体催化产生单线态氧自由基并活化表面碳结构;停止激光刺激,活化的纳米载体能持续催化产生羟自由基。这些自由基持续地激活耐药细胞内的热休克因子蛋白(heat shock factor) 的表达并形成功能性三聚体,抑制了耐药的关键信号通路;最终显著地提高肿瘤细胞内的药物蓄积量、增加药物敏感性。此外,该载体在生物体系中能很好地分散,生物相容性好,能实现温度与pH敏感的药物释放;在酸性溶酶体中,药物载体经激光刺激能产生光热效应,显著地促进了药物释放。因此,通过纳米药物载体的理性设计,结合光敏催化特性、光热效应、药物的响应释放,便能有效地逆转耐药,将为治疗耐药性的肿瘤提供全新的思路与解决方案,相关成果发表在《美国化学会会志》(J. Am. Chem. Soc. 2015, 137(5):1947-1955。本文第一作者为中科院纳米生物效应与安全性重点实验室王黎明博士,此研究是与大连理工大学、美国FDA等科研单位密切合作完成的。
近年来,陈春英课题组在纳米载体的肿瘤线粒体靶向治疗 (Nano Lett. 2011)、纳米载体光控释药 (Adv. Mater. 2012)、光热逆转肿瘤细胞耐药性 (Adv. Funct. Mater. 2014)、光热抑制肿瘤干细胞 (Biomaterials 2014)、纳米药物抑制肿瘤转移(Adv. Funct. Mater. 2014)、激光介导肿瘤靶向治疗 (J. Am. Chem. Soc. 2014)等方面取得一系列进展。在此基础上,该研究作为纳米生物医学的新发现,具有创新性和重要意义,为推动肿瘤的个性化治疗迈出坚实的一步。
该研究得到了科技部、国家自然科学基金委、中国科学院、FDA的支持。